光动力治疗(Photodynamic Therapy, PDT)是近年来兴起的一种治疗恶性肿瘤新模式,局部病灶选择性摄取光敏剂并给予适当波长的光照,通过光敏剂介导产生自由基导致氧化损伤,引起靶细胞的凋亡和坏死。因其几乎没有损伤正常组织细胞的副作用,在临床上具有独特的优势,已经在食道癌、非黑色瘤皮肤癌、宫颈癌等肿瘤的治疗中得到广泛的应用。光敏剂是光动力疗的核心,但目前临床应用的光敏剂仍存在很多不足,如种类单一、缺乏肿瘤靶向性、稳定性较差、缺乏良好的水溶性、单光子激发、分子氧依赖等。因此,研发组织穿透深度深、近红外双光子激发,可在低氧、乃至无氧条件下产生自由基的光敏剂或光活化前药具有重要意义。
大多数有机分子在光致激发后都是处于激发单重态(S1),其S1→T1系间窜越或者T1→S0辐射跃迁都是自旋禁阻的,这就造成了其三重态激发效率极低,光敏效果很不理想,单线态氧产率低下。过渡金属配合物特别是钌(II)、铱(III)等金属具有重原子效应产生的旋轨耦合,能打破S1→T1系间窜越禁阻,因而具有较大的光敏剂潜质。中山大学巢晖教授课题组在发展金属光敏剂方面开展了系列研究工作,利用金属配合物的长激发态寿命,构筑系列单/双光子光敏剂用于细胞器靶向的抗肿瘤治疗(Chem. Soc. Rev., 2021, 50, 4185; Coord. Chem. Rev., 2021, 432, 213714; Nat. Chem., 2019, 11, 1041; Nat. Commun., 2020, 11, 3262; Angew. Chem. Int. Ed., 2015, 54, 14049; 2017, 56, 14898; 2019, 58, 14334; 2020, 59, 3315; 2020, 59, 20697; 2021, 60, 4657; PNAS, 2018, 115, 5664; 2019, 116, 20296)。
近期,中山大学化学学院巢晖教授课题组与法国巴黎文理研究大学Gilles Gasser教授课题组合作,研究了一种基于内过氧化铱(III)配合物的新型光活化前药2-O-IrAn,其有效结合了乏氧双光子光敏剂和光活化化疗前药的特性。2-O-IrAn由高细胞毒性的前驱体2-IrAn,通过自发光催化内过氧化反应产生,该反应在降低2-IrAn暗毒性的同时,显著提高了其乏氧光动力治疗和光活化化疗的治疗效果。乏氧条件下,线粒体靶向的2-O-IrAn可被双光子激光活化,通过光脱笼反应释放高细胞毒性的单线态氧,同时原位将其转换回高细胞毒性的2-IrAn;或通过内过氧化物过氧键光断裂反应在线粒体原位生成高氧化能力的烷氧自由基。无论常氧还是乏氧条件下,此光活化反应都可以高效地杀伤肿瘤细胞(乏氧PI = 690.3;常氧PI = 959.1)。此外,使用DSPE-PEG-Biotin包裹的DSPE-PEG-Biotin@2-O-IrAn纳米颗粒使其具有良好的肿瘤靶向性和血液半衰期,有助于进一步的活体运用。这种近红外双光子光活化化疗和双光子光动力治疗协同作用的策略,充分彰显了DSPE-PEG-Biotin@2-O-IrAn作为抗肿瘤光活化制剂的巨大潜力,为乏氧肿瘤治疗开辟了新的道路。
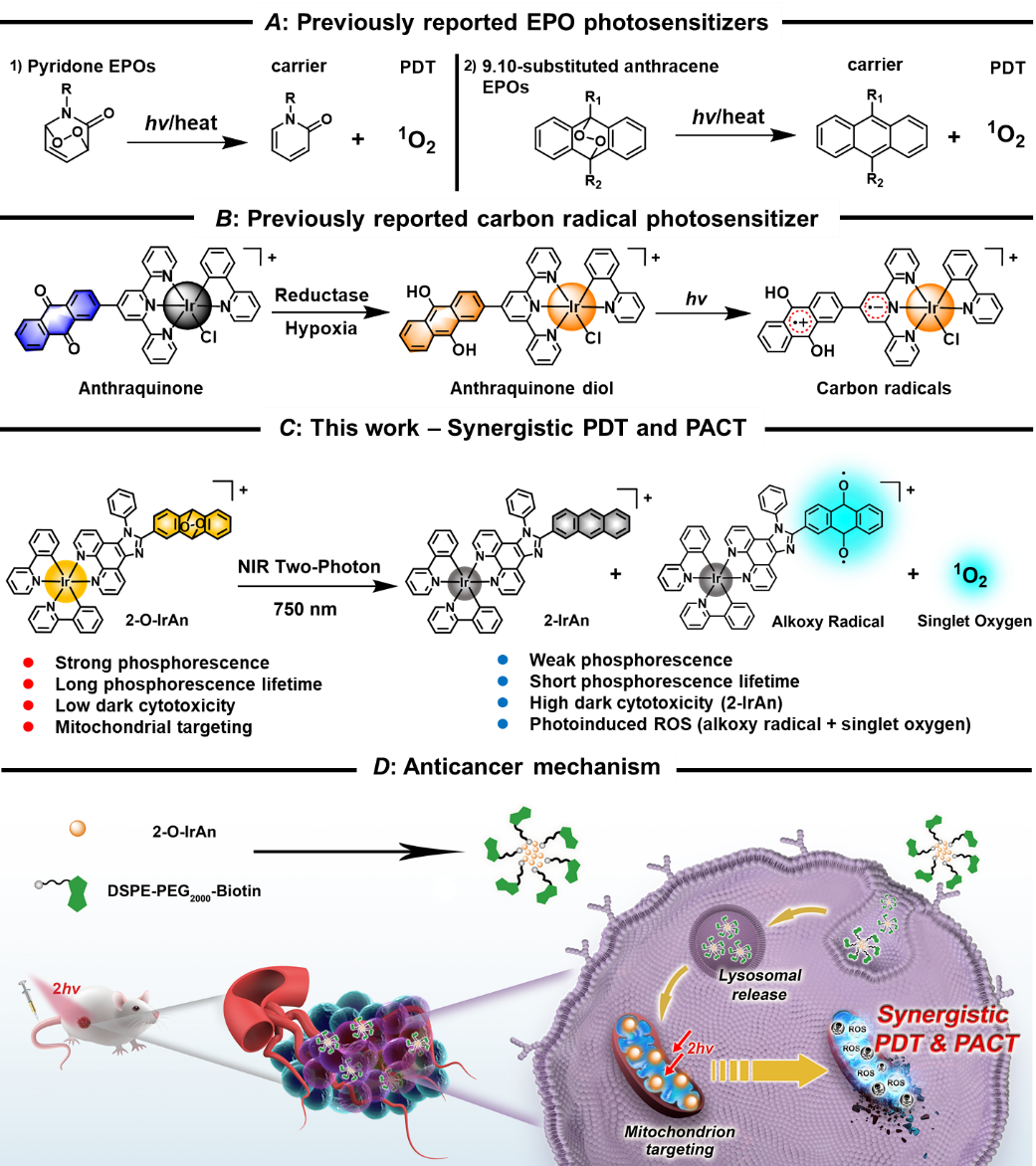

图1.(A)已报道过的内过氧化物光敏剂;(B)已报道过的铱(III)配合物碳自由基光敏剂;(C/D) 内过氧化铱(III)配合物光动力治疗和光活化化疗抗肿瘤的作用机理。
这一成果近期发表在化学综合期刊J. Am. Chem. Soc.上,题目为“Photo-Decaging of A Mitochondria-Localized Iridium(III) Endoperoxide Complex for Two-Photon Photoactivated Therapy under Hypoxia”。论文第一作者为中山大学化学学院旷实博士和博士研究生韦方棉,论文通讯作者为中山大学化学学院巢晖教授和法国巴黎文理研究大学(PSL)Gilles Gasser教授。
该研究得到国家自然科学基金(22120102002,21778079)、湖南省科技创新计划(2021RC5028)、欧洲研究委员会(GA 681679)和法国“Investissements d’Avenir”研究计划(ANR-10-IDEX-0001-02)的资助支持。