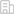抗坏血酸(H2A,又称维生素C)是一种广泛存在于各种食物中的维生素,它是一种抗氧化剂,可帮助保护细胞免受自由基的影响。近年来,抗坏血酸也被作为一种高效的促氧化剂,用于癌症治疗。然而,抗坏血酸“抗氧化”和“促氧化”作用相互“矛盾”,人们尚不清楚该生物医学功能双面性背后的分子机制,阻碍了抗坏血酸在生物医学中的应用。
由于在原子水平上具有与天然酶相似的催化中心,单原子纳米酶被视为天然酶的模拟物,被广泛应用于生物传感、药物相互作用和疾病治疗等领域。鉴于此,近日,东南大学张袁健教授课题组提出使用Fe-N-C纳米酶作为铁蛋白模拟物探索抗坏血酸催化氧化反应的机制。
该团队发现Fe-N-C纳米酶是一种多相催化剂,具有N-C和Fe-Nx两种活性位点,Fe-N-C中的Fe-Nx位点主要通过结合态中间体催化抗坏血酸氧化和四电子氧还原,同时,少量N-C位点催化二电子氧还原,催化过程中产生痕量超氧阴离子并诱导Fe-N-C中不稳定的Fe-Nx游离为Fe离子。进而,经N-C位点催化产生的过氧化氢与游离的Fe离子形成芬顿体系,衍生出一个新的四电子氧还原过程。更为重要的是,当游离的Fe离子远离催化剂时,由于抗坏血酸催化氧化过程中Fe-Nx活性位点含量的下降,更多的N-C活性位点被激活,从而直接导致过氧化氢产率上升。该研究率先发现Fe-N-C纳米酶催化抗坏血酸氧化过程中的Fe离子的析出现象,并揭示了一个新的氧气还原途径,对理解抗坏血酸促氧化效应用于清除癌细胞提供了一个新思路。

Fe-N-C纳米酶催化抗坏血酸氧化的三种路径(图片来自Angew. Chem. Int. Ed.)
东南大学化学化工学院的硕士生曹栩雯和博士生朱彩霞为本工作共同第一作者,通讯作者为化学化工学院张袁健教授和医学院沈艳飞教授,东南大学为该工作的唯一完成单位,该工作得到了国家自然科学基金的资助。