- 74 高校采购信息
- 3294 科技成果项目
- 0 创新创业项目
- 0 高校项目需求
基于高通量肿瘤转移类器官的精准用药评价平台
【痛点问题】
据世界卫生组织国际癌症研究机构(IARC)报道,中国患癌人数已居全球第一,2020年新发癌症病例457万例,癌症死亡病例300万例,其中死于恶性转移的癌症患者高达90%,因此研究癌症转移分子机制能够进一步探明恶性肿瘤的生物学本质,为精准癌症治疗提供理论依据。
近年来以类器官等拟人化模型为代表的功能性检测技术为临床研究和药物开发带来新的选择。2021年科技部下发的《关于对“十四五”国家重点研发计划6个重点专项2021年度项目申报指南征求意见的通知》中,把“基于类器官的恶性肿瘤疾病模型”列为“十四五”国家重点研发计划中首批启动重点专项任务。2021年国家药监局药审中心发布的《基因修饰细胞治疗产品非临床研究技术指导原则(试行)》中提到,当缺少相关动物模型时,可以采用类器官开展药品有效性和安全性的评估。2022年美国众议院通过法案《2022年食品和药品修正案》,首次将包括类器官在内的微生理系统作为独立的药物非临床试验评估体系纳入法案,与动物模型等视为同等重要的研究手段。
【成果介绍】
本项目组在肿瘤类器官技术的基础上首创癌症转移类器官培养系统,可根据客户提供的不同器官的CT扫描图像,利用3D打印技术制备个性化的支架,模拟相应癌组织的内部三维结构。独创的细胞外基质替代物,可发挥有效的促细胞黏附和分泌蛋白的作用,通过取代昂贵的进口胶原材料大幅降低生产和存储成本。本项目组已开发出第一代基础款骨转移和肺转移类器官培养系统,并完成高通量制备(图1),在骨肉瘤类器官和乳腺癌肺转移类器官的构建上取得成功,在特异性生物标志物的检测上与临床样品的相似度可高达80%以上。使用本产品可在体外完整重现癌细胞在转移中的形变、增殖、运动等全过程,有望逐步取代用于机制研究和药物筛选的动物模型。

核心技术包括:
① 原位癌和转移癌微环境的模拟
根据常见肿瘤转移灶的特点,本项目组使用生物材料模拟对应的组织结构和功能,再进一步进行转移癌肿瘤类器官的构建。目前已经成功构建骨肉瘤原位癌类器官、乳腺癌骨转移类器官和乳腺癌肺转移类器官。
② 复杂肿瘤类器官的构建
在新鲜肿瘤细胞经体外3D培养的基础上,通过生物医学工程手段构建包含多种细胞和组分的微生理系统,实现对肿瘤实体、免疫微环境和血管化的多角度模拟。
③ 高通量药物筛选与评价平台
利用本项目搭建的药物评价平台,模拟真实的药物测试环境,可以进行不同类型肿瘤药物的敏感性检测。本项目组开发的第一代基础款的肿瘤骨转移和肺转移类器官培养系统,初步实现了复杂肿瘤类器官的批量化构建。在特异性生物标志物的检测上与临床样品的相似度可高达80%以上,使用本产品可在体外完整重现癌细胞转移的全过程。
【竞争优势】
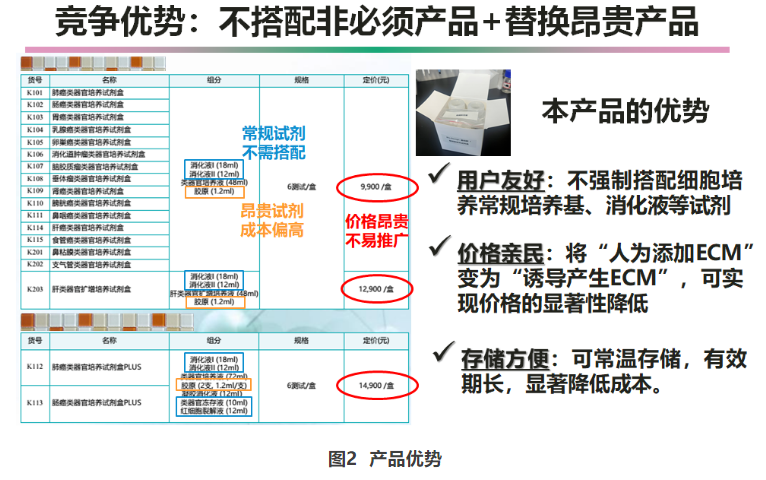
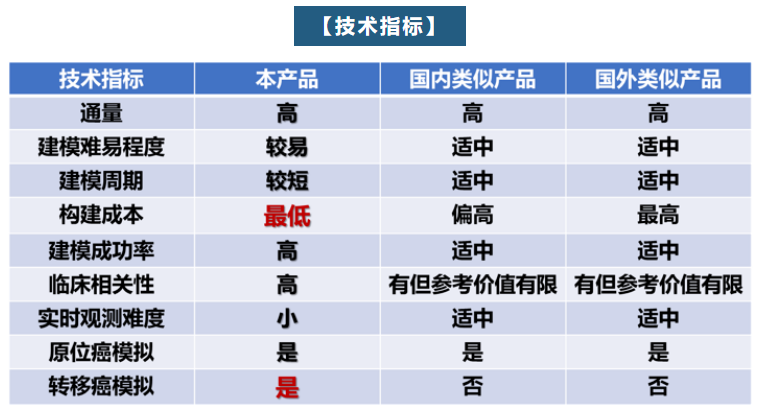
本项目组开发的肿瘤类器官,旨在实现癌症转移微环境的体外有效模拟,为抗肿瘤药物的个性化筛选提供廉价有效的新方法。凭借“用户友好、价格亲民、存储方便”三大优势(图2),更便于在科研院所、医院、制药企业推广普及。
【资质荣誉】
湖北省博士后创新创业大赛优胜奖(2023);
第九届“求是杯”大学生课外学术科技作品竞赛三等奖(2023);
第四届医学3D打印技术与临床应用全国创新大赛一等奖(2022);
华中科技大学第十二届“求是杯”大学生创业计划竞赛优秀奖(2022)。
【发展规划】
① 初期
定点选择高校、研究所、医院和制药企业,向从事癌症研究和药物筛选评价的一线研发人员提供免费的试用产品,旨在将“取代动物实验”的新型类器官产品的理念进行有效渗透,同时收集研究人员使用产品后的反馈意见。
② 发展期
经过初期的产品使用和意见反馈,对产品进行优化调整,形成行业咨询报告;积极推动“基于肿瘤转移类器官的精准用药评价平台”的商标专利和相关生产工艺的知识产权获取的进程;启动融资和生产扩大化。
③ 壮大期
利用该产品“价格低”、“货期短”、“使用方便”等优势,形成能够与进口Matrigel、Transwell等产品对峙的半壁江山;进行多轮融资,为上市做准备。
④ 成熟期
一方面将“骨转移和肺转移类器官药物评价平台”发展成国内从事癌症转移研究必备的明星产品,另一方面根据用户需求打造个性化定制方案,实现“基础研究+临床试验+市场推广+用户反馈”全流程服务;完成公司上市。
【专家介绍】

刘熙秋副教授,华中科技大学同济医学院药学院副教授,研究方向为体外疾病模型的构建。华中科技大学海外引进人才、湖北省回国科技人员创业促进会成员、欧洲癌症研究协会大使、中国生物医学工程学会高级会员、广东省精准医学应用学会类器官和器官芯片分会委员。2007年和2012年于中国科学技术大学取得生命科学学士和生物材料博士学位,2012-2016年任法国国家科学院研究员。以第一作者或通讯作者发表高水平SCI论文20余篇,其中包括Advanced Materials, Biomaterials, Journal of Controlled Release等国际一流期刊,出版英文专著1部。近5年主持国家自然科学基金2项、湖北省自然科学基金2项、华中科技大学校级基金2项,授权专利2项。担任英文期刊《Materials Today Bio》和《Acta Materia Medica》编委、广东省科技咨询专家库候选专家、中国深圳创新创业大赛评委等职务。曾获中国科学院院长奖、2021湖北省科学技术进步一等奖、第三届“花果山英才”创新创业大赛二等奖等荣誉。
在精准医疗的临床实践中,肿瘤类器官药物敏感性检测的应用场景可实现多样化:
①可根据类器官生长情况及药物敏感性检测结果,选择个性化药物方案;
②可根据患者情况向其推荐超说明书适应症的药物,基于类器官药物敏感性检测结果,综合判断超说明书适应症药物的潜在疗效;
③研究者发起的基于肿瘤类器官药物敏感性检测,指导患者个性化治疗的前瞻性临床研究。
在精准医疗时代,肿瘤靶向治疗及免疫治疗发展迅速,患者对个体化精准药物治疗的需求越来越高。采用患者肿瘤组织体外培养的类器官能很好地保留肿瘤组织的细胞结构、分子特征,且其药物敏感性检测在预测患者疗效中的准确性较高,有报道称类器官预测准确性可达80%。因此,采用肿瘤类器官指导患者治疗的需求日趋增长。
未来随着该技术的不断完善及社会大众对该领域认识逐步提高,其应用会越来越多。本项目“基于肿瘤转移类器官的精准用药评价平台”发展前景广阔,可以广泛运用于包括基础研究、药物研发、临床实践等在内的精准医疗全过程。

扫码关注,查看更多科技成果