- 74 高校采购信息
- 3294 科技成果项目
- 0 创新创业项目
- 0 高校项目需求
应用于前列腺癌荧光导航手术的靶向荧光体系S0456@PBP-EVs
PCa发病率持续快速升高,前列腺根治性切除术术中肿瘤边界判断困难所致的肿瘤残留是引起术后PCa复发和转移的关键原因。该项目在前期系列研究基础上,首次尝试利用转染PSMA配体质粒的293T细胞系制备特异性EVs作为更加安全的高特异性生物载体(PBP-EVs),并搭载高效经济NIR荧光探针S0456,从PCa细胞系和动物移植瘤水平验证其对PSMA+肿瘤靶向荧光显影特性、生物安全性及有效性。
(1)噬菌体展示技术 (Phage Display Technology, PDT)
噬菌体展示技术是将一段外源基因插入到噬菌体外壳蛋白结构基因的适当位置,在阅读框正常且不影响外壳蛋白正常功能的情况下,外源基因会随着外壳蛋白的表达而表达,从而使多肽或蛋白以融合蛋白的形式展现在噬菌体表面。通过噬菌体展示技术获得靶向PSMA的特异性的单克隆抗体及其序列,对前列腺癌研究及相关产品开发具有重要的意义。
(2)细胞外囊泡载体工程化改造及荧光探针搭载技术
EVs作为一类新型药物载体,具有良好的生物相容性,突破生理屏障的能力,优于合成载体的生物分布特征,利用细胞过程进行荧光探针搭载,利用天然细胞内运输途径的能力和表面修饰的可能性。但EVs制备难度较大,提取不当可能会导致丢失表面靶向蛋白。然而与本研究团队有良好合作关系的基础医学院黄波教授实验平台有出色的EVs研究基础,能够解决上述过程中存在的技术层面问题。
(3)近红外光下动物活体成像
荧光活体成像需要克服成像过程中面临的组织吸收、散射及自发荧光干扰等问题。本研究应用新型近红外二区荧光分子S0456,突破了传统荧光存在很强的组织吸收、散射及自发荧光干扰等瓶颈,在活体成像中可实现更高的组织穿透深度和空间分辨率。本研究团队与华中科技大学武汉光电国家研究中心张智红教授课题组拥有良好的合作关系。张智红教授课题组对于活体成像相关实验具有丰富的经验,能够解决可能出现的相关技术问题。
本项目的研究成果有望快速驱动临床转化,通过术前静脉注射荧光探针打破现有手术视觉瓶颈,实现前列腺切除术中实时、稳定、清晰的原发及转移肿瘤范围成像,以指导精准手术切除区域,最大程度避免肿瘤残留,减少术后复发,提高PCa根治治愈率。同时,该技术也能为未来人工智能肿瘤切除手术提供自主肿瘤边界范围配准奠定基础。
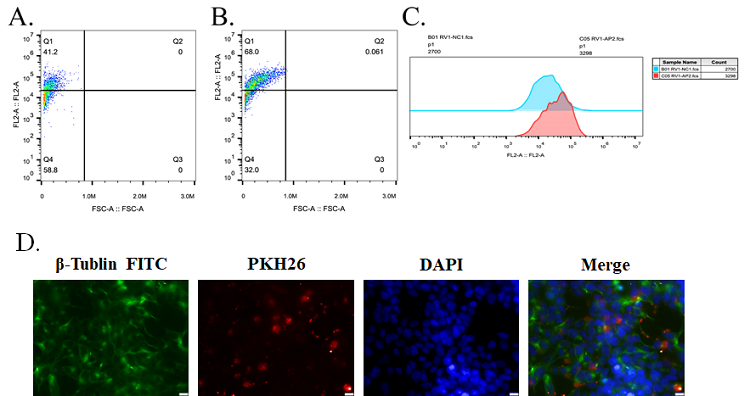
图1 前列腺癌细胞高效摄取PSMA靶向囊泡的验证
该项目旨在应用于机器人辅助腹腔镜前列腺癌荧光导航根治术领域。随着人口老龄化,前列腺癌的发病率逐年上涨,我国2019年发病率约15万人,相应的机器人手术需求量也越来越大,2020年机器人辅助腹腔镜前列腺癌根治术手术量约37,000台。因此,该项目的市场需求极大。
原理样机/验证。
目前国内市场上暂无用于机器人或腹腔镜手术中靶向示踪前列腺癌的产品,全球范围内目前仅有一款被FDA批准上市用于卵巢癌示踪的术中导航荧光探针:Cytalux(pafolacianine)。该探针依靠化学合成,产品造价高且不良反应较多;相比之下,本项目的产品应用靶向囊泡载药体系,生物相容性更好,组织穿透力和细胞摄取效率更高,且产品造价更低,性价比很高。

扫码关注,查看更多科技成果